Intestinalbarriere mit Zellen des angeborenen Immunsystems
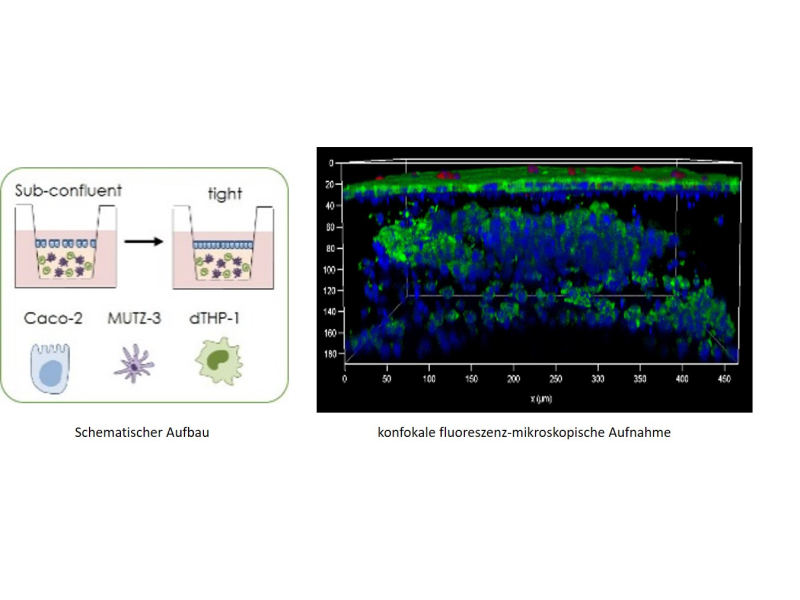
PMA-differenzierte THP-1 Zellen (Mɸ-artig, ATCC TIB-202) und MUTZ-3 (DC-artig; Deutsche Sammlung von Mikroorganismen und Zellkulturen [DSMZ], Braunschweig, Deutschland) werden in Kollagen auf Transwellinserts ausgesät und mit Caco-2 Zellen (ATCC HTB-37) (Intestinalepithel) auf der Oberfläche besät. Nach 6-7 Tagen ist die Barriere subkonfluent (5-10% offene Fläche), während die volle Ausbildung der Barriere 10-11 Tage benötigt. Das Modell kann im subkonfluenten Status zur Simulation einer chronischen Entzündung mit starker Schädigung oder im konfluenten Status zur Modellierung einer akuten Entzündung genutzt werden. Entzündung kann durch Zugabe von Zytokinen oder Toll-like-Rezeptor-Agonisten (LPS, Pam2) ausgelöst werden und führt zu einer Erniedrigung des TEER (transepithelialer elektrischer Widerstand) und Zytokinantwort.
Das Modell beruht auf humanen Zelllinien, kann aber für die Immunzellen auch mit primären Immunzellen, isoliert und differenziert aus Blutplasma, genutzt werden.
-
Hartwig O, Loretz B, Nougarede A, Jary D, Sulpice E, Gidrol X, Navarro F, Lehr CM. Leaky gut model of the human intestinal mucosa for testing siRNA-based nanomedicine targeting JAK1. J Control Release. 2022;345:646-660. doi:10.1016/j.jconrel.2022.03.037
-
Susewind J, de Souza Carvalho-Wodarz C, Repnik U, Collnot EM, Schneider-Daum N, Griffiths GW, Lehr CM. A 3D co-culture of three human cell lines to model the inflamed intestinal mucosa for safety testing of nanomaterials. Nanotoxicology. 2015:1-10. doi:10.3109/17435390.2015.1008065
-
Leonard F, Collnot EM, Lehr CM. A three-dimensional coculture of enterocytes, monocytes and dendritic cells to model inflamed intestinal mucosa in vitro. Mol Pharmaceutics. 2010;7(6):2103-2119. doi:10.1021/mp1000795
-
Hartwig O, Shetab Boushehri MA, Shalaby KS, Loretz B, Lamprecht A, Lehr CM. Drug delivery to the inflamed intestinal mucosa – targeting technologies and human cell culture models for better therapies of IBD. Adv Drug Deliv Rev. 2021;175:113828. doi:10.1016/j.addr.2021.113828
Prof. Claus-Michael Lehr: claus-michael.lehr@helmholtz-hips.de
Dr. Brigitta Loretz: brigitta.loretz@helmholtz-hips.de
Helmholtz Institut für Pharmazeutische Forschung Saarland (HIPS)
Abt. Wirkstofftransport und Biologische Barrieren
- EU-Project NEW DEAL (NMBP-2016)
- EU-Project InLiveTox (FP7)
- EU-Project MediTrans (FP6)
Ersatzmethode für Tierversuche zur Untersuchung entzündlicher Darmerkrankungen mittels chemischer Trigger
