Modellierung bakterieller Barrieren zur Untersuchung der intrazellulären Verfügbarkeit von Antiinfektiva
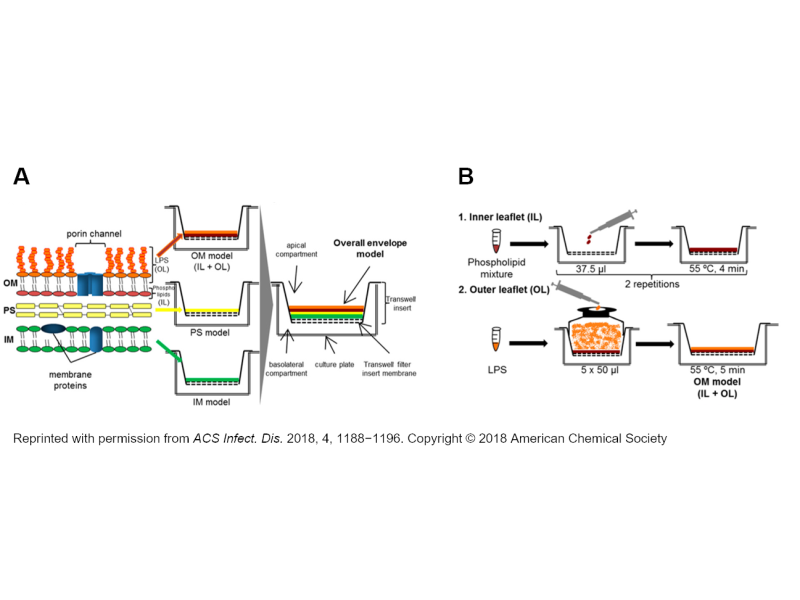
Um die aus mehreren Schichten unterschiedlicher Lipophilie aufgebaute Gram-negative Bakterienzellhülle nachzubilden, werden Transwell-Membranen zunächst mit bakteriellen Membranlipiden (z.B. POPE und POPG, 9+1) beschichtet, gefolgt von einem Alginat-Hydrogel und schließlich aus der Aerosolphase abgeschiedenen Lipopolysacchariden (LPS).
Als vereinfachtes Modell mit höherem Durchsatz kann auch lediglich eine Hydrogelbeschichtung eingesetzt werden, wobei Stärke die beste in-vitro-in-bacterio Korrelation aufweist. Umgekehrt können auch komplexere Membranmodelle durch Beschichtungen auf der Basis bakterieller Membranvesikel oder extrazellulärer Vesikel (ECVs) hergestellt werden, welche relevante Transporterproteine (z.B. Porine) enthalten.
Komplementär arbeiten wir daran, die Zellwand-Permeabilität durch Simulationsrechnungen vorherzusagen, sowie den Metabolismus von Antiinfektiva durch bakterielle Enzyme und den Einfluss von Biofilm-Polymeren in ein erweitertes Modell zur Vorhersage der bakteriellen Bioverfügbarkeit einzubeziehen.
-
Graef F, Vukosavljevic B, Michel JP, Wirth M, Ries O, De Rossi C, Windbergs M, Rosilio V, Ducho C, Gordon S, Lehr CM. The bacterial cell envelope as delimiter of anti-infective bioavailability – An in vitro permeation model of the Gram-negative bacterial inner membrane. J Control Release. 2016;243:214-224. doi:10.1016/j.jconrel.2016.10.018
-
Graef F, Richter R, Fetz V, Murgia X, De Rossi C, Schneider-Daum N, Allegretta G, Elgaher W, Haupenthal J, Empting M, Beckmann F, Brönstrup M, Hartmann R, Gordon S, Lehr CM. in vitro model of the gram-negative bacterial cell envelope for investigation of anti-infective permeation kinetics. ACS Infect Dis. 2018;4(8):1188-1196. doi:10.1021/acsinfecdis.7b00165
-
Richter R, Kamal MohamedAM, García-Rivera MA, Kaspar J, Junk M, Elgaher WAM, Srikakulam SK, Gress A, Beckmann A, Grißmer A, Meier C, Vielhaber M, Kalinina O, Hirsch AKH, Hartmann RW, Brönstrup M, Schneider-Daum N, Lehr CM. A hydrogel-based in vitro assay for the fast prediction of antibiotic accumulation in Gram-negative bacteria. Materials Today Bio. 2020;8:100084. doi:10.1016/j.mtbio.2020.100084
-
Sousa CF, Coimbra JTS, Richter R, Morais-Cabral JH, Ramos MJ, Lehr CM, Fernandes PA, Gameiro P. Exploring the permeation of fluoroquinolone metalloantibiotics across outer membrane porins by combining molecular dynamics simulations and a porin-mimetic in vitro model. BBA – Biomembranes. 2022;1864(3):183838. doi:10.1016/j.bbamem.2021.183838
-
Richter R, Kamal MAM, Koch M, Niebuur B, Huber A, Goes A, Volz C, Vergalli J, Kraus T, Müller R, Schneider‐Daum N, Fuhrmann G, Pagès J, Lehr C. An outer membrane vesicle‐based permeation assay (Ompa) for assessing bacterial bioavailability. Adv Healthcare Materials. 2022;11(5):2101180. doi:10.1002/adhm.202101180
-
Ropponen HK, Richter R, Hirsch AKH, Lehr CM. Mastering the Gram-negative bacterial barrier – Chemical approaches to increase bacterial bioavailability of antibiotics. Adv Drug Deliv Rev. 2021;172:339-360. doi:10.1016/j.addr.2021.02.014
Prof. Claus-Michael Lehr: claus-michael.lehr@helmholtz-hips.de
Dr. Brigitta Loretz: brigitta.loretz@helmholtz-hips.de
Dr. Carla Sousa: carla.sousa@helmholtz-hips.de
Glorjen Mulla: glorjen.mulla@helmholtz-hips.de
Mohamed Kamal: mohamed.kamal@helmholtz-hzi.de
Helmholtz Institut für Pharmazeutische Forschung Saarland (HIPS)
Abt. Wirkstofftransport und Biologische Barrieren
- HZI Singh-Chatwall-Fellowship (CS)
Ersatzmethode für Tierversuche zur antibakteriellen Wirkstoffforschung
Reprinted with permission from Graef F, Richter R, Fetz V, Murgia X, De Rossi C, Schneider-Daum N, Allegretta G, Elgaher W, Haupenthal J, Empting M, Beckmann F, Brönstrup M, Hartmann R, Gordon S, Lehr CM. in vitro model of the gram-negative bacterial cell envelope for investigation of anti-infective permeation kinetics. ACS Infect Dis. 2018;4(8):1188-1196. doi:10.1021/acsinfecdis.7b00165. Copyright 2018 American Chemical Society.
